Mikroben vereint gegen den Feind

Die Lebensgemeinschaft mit einem Bakterium kann Pilze vor Fressfeinden schützen – eine Erkenntnis, die neue Ansätze für eine naturnahe Landwirtschaft bietet.
10.09.2021 · News · Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie - Hans-Knöll-Institut · Fachgebiet · Lebenswissenschaften · Forschungsergebnis
Schon die kleinsten Lebewesen unserer Erde bilden höchst komplexe Beziehungsgeflechte. Mikroorganismen regeln ihre Konflikte in den Gemeinschaften über chemische Signale, die Naturstoffe. Dabei ist so mancher Akteur auf geheimer Mission.
Ungewöhnliche Parallelen
Forschende des Leibniz-Instituts für Naturstoff-Forschung und Infektionsbiologie – Hans-Knöll-Institut – (Leibniz-HKI) stießen in der Literatur auf eine auffällige Parallele: Der Pilz Mortierella verticillata soll eine giftige Substanz produzieren, die in ähnlicher Form auch von einem Bakterium gebildet wird.
„Es ist höchst unwahrscheinlich, dass so unterschiedliche Organismen wie Pilze und Bakterien solch ähnliche Stoffe bilden“, berichtet Christian Hertweck. Er ist Professor für Naturstoffchemie an der Friedrich-Schiller-Universität Jena und leitet eine Abteilung am Leibniz-HKI. Sein Team schöpfte Verdacht und machte sich auf die Spur nach einem verborgenen Mitspieler.
Tatsächlich war ein weiterer Mikroorganismus bisher undercover geblieben. Doch Hertwecks Team konnte ihn aufspüren: Mittels Fluoreszenz-Mikroskopie entdeckten die Forschenden ein bisher nicht beschriebenes Bakterium, das in den Hyphen des Pilzes lebt. Sie nannten es: Candidatus Mycoavidus necroximicus. „Der Fund befeuerte unseren Verdacht, dass nicht der Pilz das Toxin bildet, sondern das Bakterium im Innern des Pilzes“, erklärt Hannah Büttner, Doktorandin in Hertwecks Gruppe und eine der Erstautorinnen der Studie.
Detektivische Laborarbeit
Um zu untersuchen, ob tatsächlich das Bakterium für das Toxin – Necroxim genannt – verantwortlich ist, war Detektivarbeit gefragt. Das Forschungsteam führte eine Reihe vergleichender Untersuchungen im Labor durch. „Wir haben den Pilz mit Antibiotika behandelt, um den Endosymbionten, also das Bakterium im Innern des Pilzes, abzutöten. Anschließend haben wir das metabolische Profil mit dem des unbehandelten Pilzes verglichen. Bei dem bakterienfreien Pilz konnte das Necroxim nicht mehr detektiert werden“, erklärt Büttner.
Das Bakterium im Innern des Pilzes ist von ihm abhängig, sodass es ohne seinen Wirt nicht kultivierbar ist. Den Forschenden gelang es jedoch, bakterielle DNA aus den Hyphen des Pilzes zu isolieren. Aus diesen DNA-Fragmenten konnten die australischen Partner um den Molekularbiologen Sacha Pidot das gesamte Genom des Bakteriums entschlüsseln. „Das Genom des Bakteriums zeigt ein hohes Potenzial für die Synthese von Naturstoffen. Ein Gencluster kodiert außerdem Biosynthese-Enzyme, die perfekt zur Bildung von Necroxim passen“, hält Hannah Büttner fest.
Ökologische Bedeutung
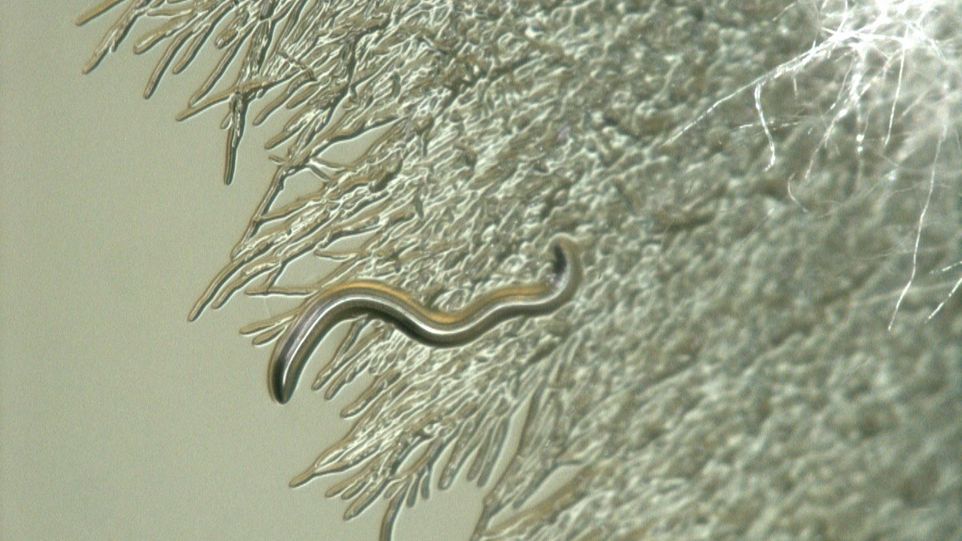
Die Forschenden nehmen an, dass der Pilz mithilfe des vom Bakterium gebildeten Toxins vor Fressfeinden wie Fadenwürmen geschützt wird, die ebenso wie der Pilz in Böden vorkommen. Bei Experimenten mit diesen Nematoden zeigte sich die toxische Wirkung: In Gegenwart der Toxin-bildenden Bakterien werden die Würmer abgetötet. Bildgebende Verfahren, die von der Forschungsgruppe um den Systembiologen Thilo Figge am Leibniz-HKI durchgeführt wurden, bestätigten die Wirkung zusätzlich.
Anwendungsmöglichkeiten
Die Entdeckung des verborgenen Bakteriums und die Entschlüsselung seiner ökologischen Funktion für den Pilz sind von großer Bedeutung. Pilze der Gattung Mortierella zeigen eine gesunde Bodenstruktur an. Sie werden in der Landwirtschaft auch als pflanzenwachstumsfördernde Pilze eingesetzt. „Unsere Ergebnisse eröffnen daher neue Ansätze für die Entwicklung natürlicher Biokontrollmittel in der Landwirtschaft“, hält Studienleiter Hertweck abschließend fest.
Die Sprache der Mikroorganismen
Die im Fachjournal PNAS veröffentlichte Studie entstand im Rahmen des von der Deutschen Forschungsgemeinschaft geförderten Sonderforschungsbereichs (SFB) „ChemBioSys“ an der Friedrich-Schiller-Universität Jena. Expertinnen und Experten aus der Mikrobiologie, Chemie und Bioinformatik beschäftigen sich seit circa acht Jahren mit komplexen mikrobiellen Lebensgemeinschaften und den chemischen Signalstoffen, die diese Beziehungen regulieren. Die Wissenschaftlerinnen und Wissenschaftler des SFB bewerben sich derzeit um eine dritte Förderperiode. Neben Hannah Büttner ist Sarah Niehs die zweite Erstautorin der Studie. Sie begann jüngst eine Tätigkeit an der Stanford University in den USA.
Publikation
Büttner H, Niehs SP, Vandelannoote K, Cseresnyés Z, Dose B, Richter I, Gerst R, Figge MT, Stinear TP, Pidot SJ, Hertweck C (2021) Bacterial endosymbionts protect beneficial soil fungus from nematode attack. Proc Natl Acad Sci U S A, 118 (37) e2110669118, doi.org/10.1073/pnas.2110669118.
